I Zasada Termodynamiki - Zrozum to Raz, a Zapamiętasz na Zawsze!
Delta U, czyli o co chodzi z tymi zmianami energii?
Wchodzimy w temat z grubej rury, bo I zasada termodynamiki to nic innego jak stwierdzenie, że energię wewnętrzną układu można zmienić na dwa sposoby: poprzez dostarczenie ciepła Q lub wykonanie pracy W. A jak to ugryźć w praktyce?
Oto I Zasada Termodynamiki w całej okazałości!
Zaczynamy od wzoru, który jest gwiazdą całego show:
ΔU = Q + W
I co to właściwie oznacza? Jeśli chcesz zmienić energię wewnętrzną układu, musisz albo dostarczyć do niego ciepło, albo wykonać nad nim pracę. Proste? No jasne, że nie... ale spokojnie, już tłumaczę! Przejdźmy do przykładu – gaz w cylindrze z ruchomym tłokiem.
Zrozum I zasadę termodynamiki na przykładzie!
Wyobraź sobie gaz zamknięty w cylindrze. Masz tłok? Masz. No to zaczynamy!
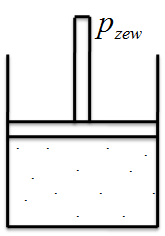
Dodaj ciepła, a cząsteczki oszaleją!
Pierwsza opcja to dostarczenie ciepła. Gdy podgrzewasz gaz, cząsteczki zaczynają tańczyć salsę – drgają, rotują, oscylują. Wynik? Ich energia wewnętrzna rośnie, bo ruch robi swoje.
Naciśnij tłok i zobacz, co się stanie!
A co, jeśli wciśniesz tłok? Nie musisz być Arnoldem Schwarzeneggerem, ale przyciśnięcie tłoku też zadziała. Zwiększasz ciśnienie, gaz się ściska, a jego energia wewnętrzna rośnie. Voilà – właśnie wykonałeś pracę nad układem!
Praca – czasem pozytywna, czasem negatywna
W wzorze ΔU = Q + W, praca może być twoim najlepszym przyjacielem albo... wrogiem.
Dodatnia praca – rośniemy!
Jeśli to Ty wykonujesz pracę nad układem, czyli np. wciskasz tłok – energia układu rośnie. Praca jest wtedy dodatnia, co oznacza, że cząsteczki są Ci wdzięczne za dodatkową energię do zabawy.
Ujemna praca – och, ulga!
Ale kiedy to układ wykonuje pracę, np. gaz rozpręża się i wypycha tłok, jego energia wewnętrzna maleje. Robi się wtedy chłodniej, a praca ma znak ujemny.
I Zasada Termodynamiki – Twoje nowe motto życiowe!
W skrócie: żeby zmienić energię wewnętrzną układu, możesz albo dostarczyć mu ciepło, albo wykonać nad nim pracę. To zasada, która rządzi światem cząsteczek i... kuchnią! Bo przecież kiedy gotujesz wodę na herbatę, to właśnie ta zasada działa w praktyce.
Chcesz wiedzieć więcej? Zajrzyj tutaj!
Zaintrygowała Cię I zasada termodynamiki? Świetnie! Na mojej stronie znajdziesz mnóstwo materiałów, które wyjaśnią Ci to jeszcze dokładniej:
- Kurs chemii fizycznej 1b: link do kursu
- Kurs termodynamiki 1a: link do kursu
A jeśli czujesz, że potrzebujesz jeszcze więcej termodynamicznej zabawy, to koniecznie sprawdź artykuł o zerowej zasadzie termodynamiki: Zerowa zasada termodynamiki




